|
|
Katalys och katalysatorer
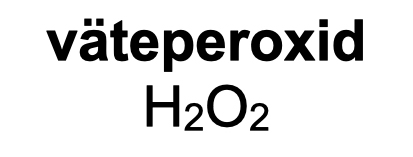
Elefanttandkräm, eller skumormen, är ett av de allra mest kända kemiexperimenten. I experimentet blandas väteperoxid (H2O2) med diskmedel och sedan sätts en lösning av kaliumjodid (KI) till. Nästan omedelbart bildas det ett tjockt skum. Väteperoxid är ett reaktivt ämne där två syreatomer sitter bundna till varandra. Detta ämne går att köpa som en utspädd vattenlösning och används till exempel till hår- eller tandblekning. Det går också att tvätta sår med väteperoxid. I mer koncentrerad form är ämnet frätande. Väteperoxid används i industrin för att bleka pappersmassa. Det är en miljövänlig blekningsmetod eftersom väteperoxiden faller sönder till vatten och syrgas. Eftersom väteperoxid är en så reaktiv molekyl är den inte stabil utan sönderfaller och bildar vatten och syrgas. Reaktionen är dock oerhört långsam. Vi kan därför ha väteperoxid i en flaska i badrummet väldigt länge utan att den sönderfaller. Men om vi häller ned kaliumjodid i väteperoxidlösningen så går reaktionen snabbt och det bildas syrgas. Syrgasen bildar sedan ett tjockt skum med diskmedlet. Det kaliumjodiden gör är att den skyndar på reaktionen. Ett sådant ämne kallas för en katalysator. En katalysator är ett ämne som påskyndar en reaktion utan att själv förbrukas. Vi säger att kaliumjodid katalyserar sönderfallet av väteperoxid. Processen kallas katalys.
Biologiska katalysatorer kallas för enzymerKatalys är väldigt vanligt i biologiska processer. Alla de kemiska reaktioner som sker i levande celler är katalyserade. Biologiska katalysatorer kallas för enzymer. Om vi till exempel lägger en tesked strösocker framför oss på bordet så vet vi att det inte kommer att reagera med luftens syre oavsett hur länge vi väntar. Om vi istället äter upp sockret så vet vi också att det kan fungera som bränsle i våra celler och generera både värme i kroppen och rörelse i våra muskler. I kroppens celler reagerar sockret med syre och bildar koldioxid och vatten i en reaktion som också frigör energi med hjälp av enzymer.
Enzymer är ofta uppbyggda av proteiner och har en komplicerad struktur. Oftast är de specialiserade på en särskild reaktion. Vi kan tänka oss enzymer som en slags molekylära maskiner. Vi stoppar in startmaterialen i ena änden och får ut produkterna i den andra. Sedan är maskinen redo för en ny omgång startmaterial. Det finns enzymer för väldigt många olika slags reaktioner. Enzymet katalas sönderdelar väteperoxid. Väteperoxid bildas ibland i levande system och därför behöver kroppen ett enzym som sönderdelar den till de ofarliga molekylerna vatten och syrgas. Ett annat exempel på katalys i kroppen är enzymet laktas som katalyserar nedbrytningen av mjölksocker. Det kemiska namnet för mjölksocker är laktos. Laktas saknas hos personer som är laktosintoleranta och de kan därför inte bryta ned laktos i tunntarmen. Eftersom laktos inte bryts ned som den borde i tunntarmen kommer den istället att brytas ned av bakterier i tjocktarmen. Denna nedbrytning ger upphov till gaser i magen. Laktos i tjocktarmen ger också diarré eftersom tjocktarmen inte kan ta upp lika mycket vatten som den brukar.
Katalysatorer används för att ta bort skadliga ämnen i bilavgaser
Katalysatorer används också i bilar. I avgaserna från förbränningsmotorer i bilar finns det kolmonoxid, kolväten och kväveoxider som är skadliga för människa och miljö. Dessa gaser bryts ned mycket långsamt. Med hjälp av en katalysator reagerar kolmonoxid, kolväten och kväveoxiderna och bildar vatten, koldioxid och kvävgas. Katalysatorn består av ädelmetallerna platina och rodium.
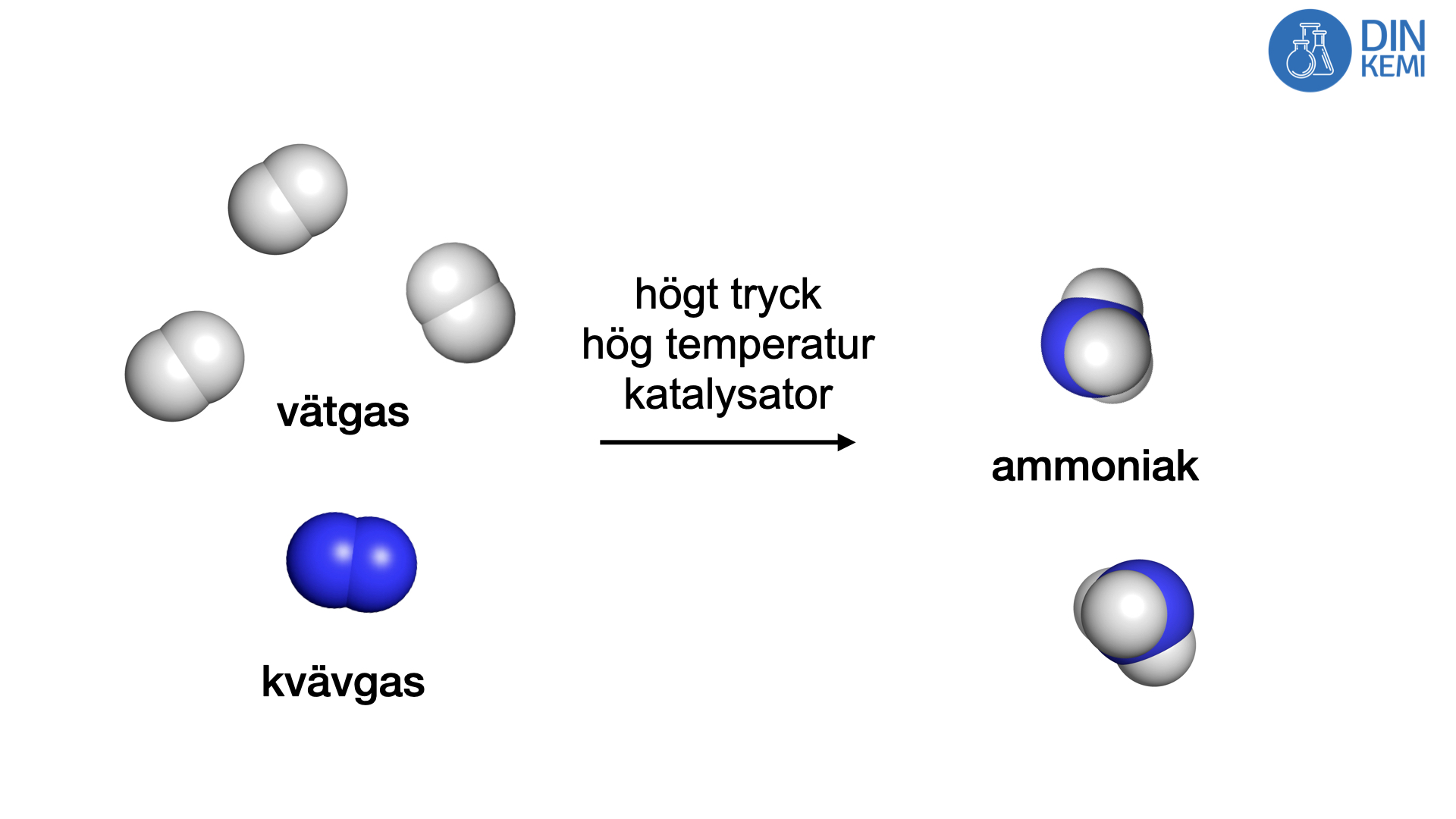
Industriella katalysatorer är viktiga för samhälletKatalys är oerhört viktigt i industriella tillämpningar för att framställa molekyler och material som behövs i det moderna samhället. En uppskattning är att katalys direkt eller indirekt bidrar till ungefär 35 % av världens samlade BNP. Ett exempel på industriprocesser som använder katalys är den så kallade Haber-Boschprocessen. I Haber-Boschprocessen omvandlas kvävgas och vätgas till ammoniak under högt tryck med hjälp av en järnbaserad katalysator. Ammoniak utgör huvudbeståndsdelen i konstgödning. Konstgödning är basen för mycket av vår matproduktion. Du äter alltså alltid mat som innehåller kväveatomer som kommer från Haber-Boschprocessen. En uppskattning är att 40 % av kväveatomerna i din kropp kommer från insidan av en Haber-Boschreaktor. Kväveatomerna finns framförallt i proteiner och DNA.
När Fritz Haber och Carl Bosch utvecklade den här processen i 1910-talets Tyskland så var de inte bara intresserade av att göra gödningsmedel utan de ville också hitta ett sätt för Tyskland att göra sprängämnen. Vid sprängämnesproduktion omvandlas ammoniaken till salpetersyra och då används också katalys. Även idag tillverkas det sprängämnen av ammoniak men ungefär 90 % av ammoniakproduktionen går till konstgödning. Både Fritz Haber och Carl Bosch fick nobelpris för sina upptäckter.
Många plaster tillverkas med hjälp av katalysatorerEn annan viktig industriell process som är beroende av katalys är plasttillverkning. Sedan början av 1900-talet har enkla kolväten såsom eten, propen och butadien tillverkats direkt från olja. Sedan används dessa för att göra en mängd olika kemikalier. Inledningsvis var det inte möjligt att göra hårdplast av eten och propen utan för det krävdes mer komplicerade startmaterial. År 1953 lyckades Karl Ziegler och hans medarbetare omvandla eten till högdensitetspolyeten (HDPE) och sedan också propen till polypropen (PP).
Många av de plastprodukter som används till livsmedel är gjorda av HDPE eller PP. Vid tillverkningen används en titankatalysator med helt enastående effektivitet. Det är en av de mest effektiva katalysatorerna. Det behövs så otroligt lite av den att det inte går att separera katalysatorn från den färdiga plasten. Därför innehåller dessa plastartiklar alltid en liten rest av titan (Ti). Mängden är ungefär en miljondel. Haber, Bosch och Ziegler fick alla nobelpris för sina upptäckter. Uppskattningsvis har var femte nobelpristagare i kemi fått priset för arbete kring katalys.
Quiz - Katalys och katalysatorerUppgifter - Katalys och katalysatorer
Förklara och beskriv
Argumentera och resonera
Ta reda på
|